
Поиски «эликсира молодости» продолжаются тысячи лет, но существенно удлинить человеческую жизнь не удалось пока ни магам, ни алхимикам. Несколько больше надежд дают недавние биологические открытия: по крайней мере теперь мы лучше понимаем, как устроено старение и что ему можно противопоставить. Некоторые из действительно работающих стратегий борьбы связаны с изменением образа жизни. Это и ограничение потребления калорий, и интервальное голодание, и физическая активность. Все они по крайней мере частично направлены на усиление аутофагии — процесса, который нередко называют «контролируемым самоубийством» клетки. Он является важнейшей частью ее нормальной жизни, позволяя избавляться от внутриклеточных патогенов, уничтожать поврежденные белки и органеллы прежде, чем они нанесут ущерб.
Аутофагия клеток в мозге замедляет накопление белковых агрегатов — бета-амилоида и тау-белка (при болезни Альцгеймера) и телец Леви (при паркинсонизме). Включаясь в пораженных инфекцией клетках, она поставляет иммунной системе образцы молекул патогена для развития эффективного ответа. Имеются данные о связи нарушения аутофагии с развитием ожирения и диабета II типа. Но главное для нас — то, что ее замедление происходит в стареющем организме: недаром для пожилого возраста так характерны все перечисленные выше заболевания. Считается, что стимуляция этих процессов позволит замедлить старение и увеличить продолжительность жизни, а один из перспективных инструментов запуска аутофагии — ограничение потребления калорий.

Самодисциплина для самоисцеления
Эффективность умеренного голодания многократно показана в экспериментах на самых разных модельных организмах, от дрожжей и нематод до грызунов и макак. Однако добиться от людей добровольного самоограничения оказалось куда сложнее. Недаром, несмотря на все доводы медиков, число людей с избыточным весом за последние 40 лет почти утроилось. По оценкам ученых из Гарвардской школы общественного здравоохранения, более 57% нынешних американских детей уже к 35 годам будут страдать ожирением. Каждый, кто клялся себе начать с понедельника новую жизнь, знает, как тяжело дается дисциплина. Вот если бы можно было просто проглотить таблетку!
Как ни странно, это вполне возможно: так работают миметики ограничения калорий (Calorie restriction mimetics, CRM) — соединения, имитирующие эффекты голодовки. Первыми и самыми простыми из них оказались антигликолитики, подавляющие усвоение из пищи высокоэнергетических жиров и углеводов. Однако их влияние на организм чересчур сложно, что приводит к многочисленным и часто опасным побочным эффектам. По счастью, сигнальные пути, участвующие в запуске аутофагии (в том числе и в ответ на нехватку пищи), установлены достаточно детально. Мы можем целенаправленно искать вещества, избирательно действующие на нужные этапы этого процесса и вовлеченные в него белки.
Звенья гибельной цепи
Например, пока питательных веществ хватает, в клетке сохраняется достаточно аденозинтрифосфата (АТФ), ацетилкофермента А (ацетил-КоА) и восстановленного никотинамидадениндинуклеотида (NADH) — важнейших участников метаболизма. Присутствие этих веществ напрямую ингибирует работу некоторых ключевых белков аутофагии, таких как сиртуины. Другие подавляются ферментом Р300, который реагирует на присутствие ацетил-КоА, третьи «выключаются» рецепторами межклеточных гормонов, факторов роста. Нехватка питания, которая приводит к уменьшению запасов АТФ, ацетил-КоА и NADH, отсутствие факторов роста и дезактивация белка Р300, не получающего ацетил-КоА, — все это запускает «самопереваривание» и обновление клетки. Каждое из этих звеньев может стать целью для воздействия CRM-препаратов.
Исследования CRM лишь начинаются: окончательных доказательств их пользы для организма пока нет. И уж тем более не существует фармакологических средств, которые использовали бы CRM; встречающиеся в продаже всевозможные биологически активные добавки и чудодейственные травяные препараты к таковым отнести нельзя. Однако медики уже определили некоторые вещества, способные влиять на работу регуляторных механизмов аутофагии, и продолжают изучать их эффекты, будь то снижение содержания в клетке небольших молекул ацетил-КоА или NADH или регуляция ферментов. Попробуем рассмотреть оба метода имитации.
Метод малых молекул
Ацетил-КоА производится ферментом цитратлиазой при расщеплении питательных углеводов. Работу этого белка подавляет гидроксицитрат, содержащийся в карри (плоды гарцинии камбоджийской) и каркаде (отвар гибискуса) — и в бесчисленных «жиросжигающих» БАДах недоказанного действия. В самом деле, гидроксицитрат снижает синтез ацетил-КоА, и эксперименты показали, что под его действием замедляется накопление жировых капель в куриных гепатоцитах, а у крыс усиливается метаболизм белков. Однако к людям это почти не относится: если вещество и обладает каким-то эффектом, то очень небольшим и краткосрочным.
Аутофагия не всегда благо
Так, на первых стадиях развития рака она позволяет укротить этот процесс, сдерживая рост и деление переродившихся клеток. Но на поздних этапах аутофагией может вооружиться уже сама опухоль, используя ее для переваривания окружающих тканей и питания.
Другой вариант — влияние на уровень NADH. Эти молекулы синтезируются клеткой из витамина В3 — никотинамида и близких к нему соединений, таких как рибозид никотинамида или никотиновая кислота. Теоретически целенаправленный прием этих препаратов может обеспечить поддержание нужного количества NADH в клетках. И действительно, показано, что никотинамида рибозид может предотвращать дегенерацию нейронов; никотинамид поддерживает функционирование сердца при кардиомиопатии. Но спешить за такими БАДами также пока рано: нужные исследования проведены лишь на культурах клеток и животных моделях.
В медицинской практике применяется разве что никотиновая кислота, которую используют для нормализации жирового обмена. Однако это не гарантирует ее эффективности в предотвращении сердечно-сосудистых заболеваний, а тем более в замедлении процессов старения. Что бы ни обещали производители БАДов, этот способ имитации голода лишь прорабатывается учеными. Но как дела с другим? В конце концов, тот же уровень NADH влияет на аутофагию, меняя активность сиртуинов и других белков, — и CRM способен воздействовать непосредственно на них.
Метод регуляции белков
Активность сиртуинов можно регулировать некоторыми полифенолами, включая такое известное соединение, как ресвератрол, содержащееся в винограде, орехах, зеленом чае и красном вине. В самом деле, ресвератрол считается возможной причиной «французского парадокса» — довольно низкого уровня коронарной болезни сердца на фоне диеты, богатой холестерином и насыщенными жирами животных. Имеются данные о положительном влиянии ресвератрола и на кишечную микрофлору, и на восстановление нейронов у модельных мышей с болезнью Альцгеймера. Положительные результаты дают и некоторые клинические эксперименты. Так, у принимавших ресвератрол пациентов с диабетом II типа значительно уменьшились показатели маркеров окислительного стресса, а также индекс массы тела и кровяное давление.
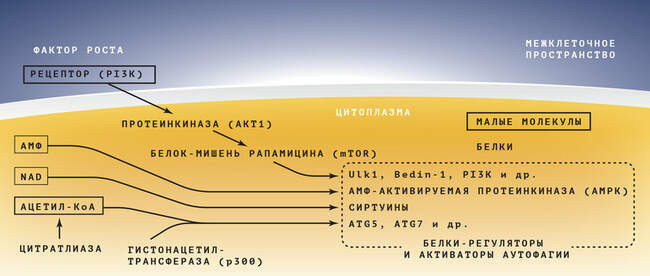
Ключевые регуляторы аутофагии
Запустить аутофагию можно, имитируя дефицит калорий — воздействуя на внутриклеточный уровень ацетил-КоА, NADH или напрямую на белки, участвующие в этом процессе.
Другой белковой мишенью может стать фермент P300 — белок, регулирующий работу массы генов клетки. Веществ, которые могут влиять на его активность, тьма, и изучены они лучше всех. Например, для гарцинола (содержится в карри) уже продемонстрировано антиоксидантное, противомикробное, противораковое действие и накоплено столько исследований «в пробирке» и на животных моделях, что осталось проверить его фармакокинетику — и можно переходить к клиническим испытаниям. Не отстает и куркумин — его антибактериальные свойства открыли еще в 1949 году, и к нашему времени получено немало результатов исследований как на животных, так и на людях. А спермидин (соя, дуриан, яблоки, брокколи) недавно удостоился большого обзора в журнале Science: исследования позволяют считать, что его потребление коррелирует со снижением смертности от сердечно-сосудистых заболеваний и рака.

Однако наиболее признанными веществами из нашего списка CRM пока что остаются ингибиторы mTOR — прежде всего рапамицин, нашедший применение в качестве иммунодепрессанта. К сожалению, средством продления жизни сам по себе он не станет: при продолжительном получении рапамицин начинает воздействовать на mTOR в составе других белковых комплексов, ведя к тяжелым побочным эффектам. Поиск «рапалогов», аналогов рапамицина, которые будут действовать лишь на нужный белковый комплекс mTOR, еще продолжается.
Установить факторы, влияющие на продолжительность человеческой жизни, чрезвычайно сложно: уж слишком их много, и слишком они разнообразны. Особенно нелегко выяснить эффекты отдельных веществ из всего многообразия, поступающего в организм с пищей. Недаром почти все CRM применяются пока что лишь в составе добавок сомнительного происхождения. Но ученые продолжают работу, и, возможно, вскоре такие препараты войдут в область доказательной медицины, а на полках аптек появятся эффективные «имитаторы голода» — долгожданные таблетки от старости. Ну а пока этот момент не настал, нам остается старый добрый метод самоограничений и самодисциплины.

























